Sabemos que na natureza, tudo tende à uma certa desordem. O esforço para manter as coisas organizadas é sempre maior do que para que elas fiquem desorganizadas (é só a gente pensar onde guardamos nossas roupas que confirmamos isso!). Na termodinâmica, existe um nome para isso: Entropia (S) – Grau de desordem do sistema.
Quando uma substância é aquecida, suas moléculas se agitam, e a entropia aumenta. Quando é resfriada, a entropia diminui. E se não há troca térmica, a entropia permanece constante. Podemos colocar da seguinte forma:
- Recebe calor – ΔS > 0
- Cede calor – ΔS < 0
- Adiabático – ΔS = 0
Rudolf Clausius definiu a variação de entropia de um sistema como:
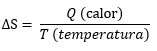
Vale a observação que, olhando o Universo como um sistema, a entropia sempre aumenta. Imagine a fabricação de lingotes de aço para a construção de um edifício. Usa-se o minério para formar uma estrutura ordenada. Porém, para poder fabricar os lingotes, precisamos fazer a extração desse minério, o que causa uma grande desordem. Olhando o sistema como um todo, não apenas a construção do edifício ou a fabricação do lingote, a desordem causada para extrair o minério é maior, ou seja, a desordem, a entropia, sempre aumenta.
Acesse uma questão resolvida sobre esse assunto aqui: Exercício ENEM 2016.

1 comentário